Se non sbaglio sia il 7-keto che il 7-OH sono stati bannati. Ragazzi posso spiegarvi le differenze tra le due molecole, ma per comprenderle meglio occorrono delle basi di chimica e biochimica.
Sono molecole simili tra loro, o meglio, il 7-keto dhea (o 7-oxo dhea) rappresenta la forma ossidata (in C-7) del 7-OH dhea (o 7-idrossi-dhea). Viceversa il 7-OH dhea rappresenta la forma ridotta del 7-keto dhea. L'interconversione tra le due forme di questi steroidi è catalizzata dall'enzima 11-beta-idrossisteroide-deidrogenasi 1 (11-beta HSD1), enzima NADPH dipendente. Questo è lo stesso enzima che catalizza la conversione periferica (in diversi tessuti, quali fegato e tessuto adiposo) del cortisone (forma ossidata di questo glucocorticoide) in cortisolo (forma ridotta), che è la forma biologicamente attiva di questo ormone.

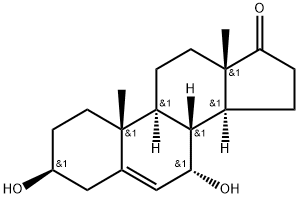

7-OH DHEA --------------------------- 7-KETO DHEA
Sia il 7-Keto che il 7-Oh si comportano da inibitori dell'enzima 11-beta HSD1.
Un inibitore enzimatico può essere competitivo, non competitivo o misto. Un inibitore competitivo compete con il substrato (in questo caso il cortisone) nel legarsi al sito attivo (catalitico) dell'enzima ed è tanto più efficace quanto più alta è la sua affinità nei confronti dell'enzima rispetto al substrato originario. L'inibitore competitivo quindi, si lega all'enzima impedendo che lo faccia il substrato originario, sottraendo quindi molecole di enzima disponibili a catalizzare la reazione originaria (in questo caso la conversione del cortisone in cortisolo).
Un inibitore non competitivo o un inibitore di tipo misto invece, possono legarsi sia all'enzima e sia al complesso enzima-substrato (in questo caso l'11-beta-HSD1 e il cortisone), poichè si legano a siti diversi dal sito attivo dell'enzima. Legandosi al complesso ES impediscono che l'enzima termini la sua reazione, ovvero fanno tornare la reazione indietro. L'efficacia di un'inibitore è misurata tramite una costante, Ki. Quanto più basso è il valore di Ki, tanto più è efficace l'inibitore.
Il 7-Oh Dhea, in entrambe le forme isomeriche (7-alfa-Oh e 7-beta-Oh), è un inibitore competitivo dell'enzima 11-beta-HSD1, mentre il 7-keto dhea è un inibitore di tipo misto di questo enzima.
Ma la cosa più importante, è che il 7-Oh, specie l'isomero beta (che poi era quello contenuto nel lean xtreme), ha una Ki minore rispetto al 7-keto. Ciò significa che il 7-beta-Oh è molto più efficace del 7-keto nell'inibire la conversione periferica del cortisone in cortisolo.
Dehydroepiandrosterone 7alpha-hydroxylation in human tissues: possible interference with type 1 11beta-hydroxysteroid dehydrogenase-mediated processes.
Hennebert O, Chalbot S, Alran S, Morfin R.
Source
Laboratoire de Biotechnologie, EA-3199, Conservatoire National des Arts et Métiers, 2 rue Conté, 75003 Paris, France.
Abstract
Dehydroepiandrosterone (DHEA) is 7alpha-hydroxylated by the cytochome P450 7B1 (CYP7B1) in the human brain and liver. This produces 7alpha-hydroxy-DHEA that is a substrate for 11beta-hydroxysteroid dehydrogenase type 1 (11beta-HSD1) which exists in the same tissues and carries out the inter-conversion of 7alpha- and 7beta-hydroxy-DHEA through a 7-oxo-intermediary. Since the role of 11beta-HSD1 is to transform the inactive cortisone into active cortisol, its competitive inhibition by 7alpha-hydroxy-DHEA may support the paradigm of native anti-glucocorticoid arising from DHEA. Therefore, our objective was to use human tissues to assess the presences of both CYP7B1 and 11beta-HSD1. Human skin was selected then and used to test its ability to produce 7alpha-hydroxy-DHEA, and to test the interference of 7alpha- and 7beta-hydroxy-DHEA and 7-oxo-DHEA with the 11beta-HSD1-mediated oxidoreduction of cortisol and cortisone. Immuno-histochemical studies showed the presence of both CYP7B1 and 11beta-HSD1 in the liver, skin and tonsils. DHEA was readily 7alpha-hydroxylated when incubated using skin slices. A S9 fraction of dermal homogenates containing the 11beta-HSD1 carried out the oxidoreduction of cortisol and cortisone. Inhibition of the cortisol oxidation by 7alpha-hydroxy-DHEA and 7beta-hydroxy-DHEA was competitive with a Ki at 1.85+/-0.495 and 0.255+/-0.005 microM, respectively. Inhibition of cortisone reduction by 7-oxo-DHEA was of a mixed type with a Ki at 1.13+/-0.15 microM. These findings may support the previously proposed native anti-glucocorticoid paradigm and suggest that the 7alpha-hydroxy-DHEA production is a key for the fine tuning of glucocorticoid levels in tissues.
Sono molecole simili tra loro, o meglio, il 7-keto dhea (o 7-oxo dhea) rappresenta la forma ossidata (in C-7) del 7-OH dhea (o 7-idrossi-dhea). Viceversa il 7-OH dhea rappresenta la forma ridotta del 7-keto dhea. L'interconversione tra le due forme di questi steroidi è catalizzata dall'enzima 11-beta-idrossisteroide-deidrogenasi 1 (11-beta HSD1), enzima NADPH dipendente. Questo è lo stesso enzima che catalizza la conversione periferica (in diversi tessuti, quali fegato e tessuto adiposo) del cortisone (forma ossidata di questo glucocorticoide) in cortisolo (forma ridotta), che è la forma biologicamente attiva di questo ormone.


7-OH DHEA --------------------------- 7-KETO DHEA
Sia il 7-Keto che il 7-Oh si comportano da inibitori dell'enzima 11-beta HSD1.
Un inibitore enzimatico può essere competitivo, non competitivo o misto. Un inibitore competitivo compete con il substrato (in questo caso il cortisone) nel legarsi al sito attivo (catalitico) dell'enzima ed è tanto più efficace quanto più alta è la sua affinità nei confronti dell'enzima rispetto al substrato originario. L'inibitore competitivo quindi, si lega all'enzima impedendo che lo faccia il substrato originario, sottraendo quindi molecole di enzima disponibili a catalizzare la reazione originaria (in questo caso la conversione del cortisone in cortisolo).
Un inibitore non competitivo o un inibitore di tipo misto invece, possono legarsi sia all'enzima e sia al complesso enzima-substrato (in questo caso l'11-beta-HSD1 e il cortisone), poichè si legano a siti diversi dal sito attivo dell'enzima. Legandosi al complesso ES impediscono che l'enzima termini la sua reazione, ovvero fanno tornare la reazione indietro. L'efficacia di un'inibitore è misurata tramite una costante, Ki. Quanto più basso è il valore di Ki, tanto più è efficace l'inibitore.
Il 7-Oh Dhea, in entrambe le forme isomeriche (7-alfa-Oh e 7-beta-Oh), è un inibitore competitivo dell'enzima 11-beta-HSD1, mentre il 7-keto dhea è un inibitore di tipo misto di questo enzima.
Ma la cosa più importante, è che il 7-Oh, specie l'isomero beta (che poi era quello contenuto nel lean xtreme), ha una Ki minore rispetto al 7-keto. Ciò significa che il 7-beta-Oh è molto più efficace del 7-keto nell'inibire la conversione periferica del cortisone in cortisolo.
Dehydroepiandrosterone 7alpha-hydroxylation in human tissues: possible interference with type 1 11beta-hydroxysteroid dehydrogenase-mediated processes.
Hennebert O, Chalbot S, Alran S, Morfin R.
Source
Laboratoire de Biotechnologie, EA-3199, Conservatoire National des Arts et Métiers, 2 rue Conté, 75003 Paris, France.
Abstract
Dehydroepiandrosterone (DHEA) is 7alpha-hydroxylated by the cytochome P450 7B1 (CYP7B1) in the human brain and liver. This produces 7alpha-hydroxy-DHEA that is a substrate for 11beta-hydroxysteroid dehydrogenase type 1 (11beta-HSD1) which exists in the same tissues and carries out the inter-conversion of 7alpha- and 7beta-hydroxy-DHEA through a 7-oxo-intermediary. Since the role of 11beta-HSD1 is to transform the inactive cortisone into active cortisol, its competitive inhibition by 7alpha-hydroxy-DHEA may support the paradigm of native anti-glucocorticoid arising from DHEA. Therefore, our objective was to use human tissues to assess the presences of both CYP7B1 and 11beta-HSD1. Human skin was selected then and used to test its ability to produce 7alpha-hydroxy-DHEA, and to test the interference of 7alpha- and 7beta-hydroxy-DHEA and 7-oxo-DHEA with the 11beta-HSD1-mediated oxidoreduction of cortisol and cortisone. Immuno-histochemical studies showed the presence of both CYP7B1 and 11beta-HSD1 in the liver, skin and tonsils. DHEA was readily 7alpha-hydroxylated when incubated using skin slices. A S9 fraction of dermal homogenates containing the 11beta-HSD1 carried out the oxidoreduction of cortisol and cortisone. Inhibition of the cortisol oxidation by 7alpha-hydroxy-DHEA and 7beta-hydroxy-DHEA was competitive with a Ki at 1.85+/-0.495 and 0.255+/-0.005 microM, respectively. Inhibition of cortisone reduction by 7-oxo-DHEA was of a mixed type with a Ki at 1.13+/-0.15 microM. These findings may support the previously proposed native anti-glucocorticoid paradigm and suggest that the 7alpha-hydroxy-DHEA production is a key for the fine tuning of glucocorticoid levels in tissues.


 )
)
Commenta